这个条目来自axispharm
谷氨酰胺代谢在癌症生长、能量产生和生物合成中起着关键作用。自1935年汉斯·克雷布斯首次描述三羧酸(TCA)循环以来,研究强调了谷氨酰胺在正常细胞和癌细胞中的重要性。今天,在癌症治疗中靶向谷氨酰胺途径显示出有希望的潜力。该指南解释了谷氨酰胺的影响,它在自噬和活性氧中的作用,针对它的策略,以及未来治疗的考虑。
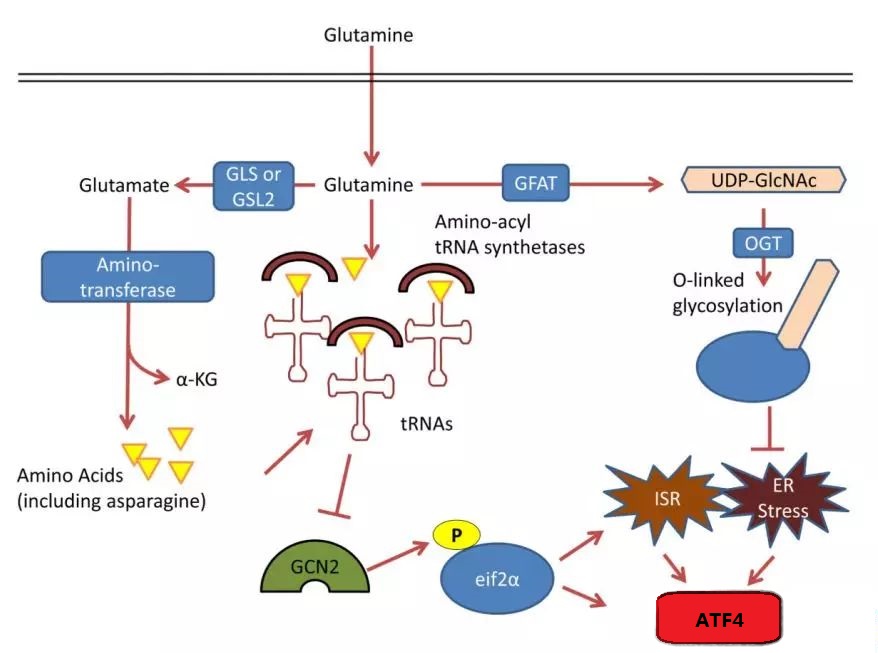
核酸、脂质和蛋白质中谷氨酰胺的合成
1. 癌细胞中的谷氨酰胺代谢
癌细胞严重依赖谷氨酰胺:
- 能源生产:谷氨酰胺为TCA循环提供燃料,转化为α-酮戊二酸提供能量。
- 生物合成:它为构建核苷酸、脂质和蛋白质提供碳和氮。
- 代谢灵活性:当营养物质缺乏时,癌细胞会转而使用谷氨酰胺作为能量来源。
癌细胞使用几种策略来获得谷氨酰胺:
- 高摄取量:它们通过SLC1A5这样的转运蛋白吸收谷氨酰胺。
- 营养清除:在应激状态下,细胞分解内部成分或吞噬蛋白质以获得谷氨酰胺。
2. 谷氨酰胺在生物合成中的作用
-
核酸合成
- 谷氨酰胺为制造嘌呤和嘧啶提供氮。没有它,癌细胞可能会停止分裂。
- 它激活mTOR途径,刺激参与核苷酸生产的酶。
-
脂质合成
- 谷氨酰胺衍生的α-酮戊二酸转化为乙酰辅酶a,支持脂质形成。
-
蛋白质合成
- 谷氨酰胺为氨基酸提供氮,并帮助蛋白质折叠。低水平会导致蛋白质压力。
3. 谷氨酰胺代谢途径
-
TCA循环和IDH2
- 在TCA循环中,谷氨酰胺衍生的α-酮戊二酸转化为异柠檬酸和柠檬酸。酶IDH2有助于这一过程,促进能量产生。
- IDH2的突变可以破坏谷氨酰胺代谢,影响癌症生长。
-
谷胱甘肽途径
- 谷氨酰胺代谢产生谷氨酸,是谷胱甘肽的前体。这种抗氧化剂可以中和有害的活性氧(ROS)。
- 通过谷氨酰胺代谢产生的NADPH支持谷胱甘肽再生,有助于控制活性氧水平。
4. 谷氨酰胺和自噬在癌症研究中的作用
谷氨酰胺在自噬中起着重要作用,自噬是细胞分解自身成分获取营养的过程:
- 提高癌症存活率:当营养物质不足时,谷氨酰胺支持自噬,让癌细胞自我维持。
- 在肿瘤生长中的双重作用:自噬既可以帮助肿瘤生长,也可以阻碍肿瘤生长。虽然它可以减少氧化压力,防止染色体不稳定,但它也有助于癌细胞在压力下生存。
- 与压力通路相互作用:谷氨酰胺通过mTOR和GCN2等途径影响自噬,促进营养摄入和管理细胞应激。
5. 谷氨酰胺和活性氧在癌症研究中的作用
谷氨酰胺和活性氧
癌细胞需要控制活性氧水平以避免损伤:
- 中等活性氧水平:低至中等水平通过细胞分裂信号促进细胞生长。
- 高活性氧水平:过多的ROS会损伤细胞,导致细胞死亡。癌细胞需要小心平衡活性氧以避免伤害。
- 用谷氨酰胺调节活性氧:通过代谢,谷氨酰胺生成谷胱甘肽和NADPH。两者对于中和活性氧和保护细胞免受损伤都是至关重要的。
- 影响肿瘤微环境:谷氨酰胺衍生的代谢物有助于控制肿瘤微环境中的ROS,帮助癌细胞适应和存活。
6. 谷氨酰胺和T细胞
谷氨酰胺不仅对癌细胞重要。它还刺激免疫细胞,尤其是T细胞:
- 早期激活:在活化过程中,T细胞需要谷氨酰胺才能快速生长和分裂。它提供能量和基本的建筑材料。
- t细胞分化:谷氨酰胺影响CD4+ T细胞如何发育成不同的亚型,从而影响免疫反应。
7. 靶向谷氨酰胺代谢的策略
扰乱谷氨酰胺代谢会削弱癌细胞:
- 谷氨酰胺酶抑制剂(如CB-839):这些药物阻断谷氨酰胺酶,阻止谷氨酰胺转化为谷氨酸。
- 转运蛋白抑制剂:靶向谷氨酰胺转运蛋白如SLC1A5会减少谷氨酰胺的摄取,剥夺细胞的营养。
- 联合治疗:谷氨酰胺抑制剂与化疗、免疫疗法或IDH2抑制剂联合使用可提高疗效。
8. 谷氨酰胺靶向治疗的关键考虑
谷氨酰胺酶抑制剂的临床应用
-
代谢灵活性
- 癌细胞通过转换代谢途径来适应营养变化。了解这些变化可以发现新的治疗方法。
-
肿瘤微环境
- 缺氧和酸度等因素会影响细胞如何利用谷氨酰胺。增加改变肿瘤环境的疗法可能会提高疗效。
-
谷氨酰胺成瘾
- 一些肿瘤严重依赖谷氨酰胺。将谷氨酰胺靶向治疗与癌基因抑制剂结合可能产生合成致死性。
-
靶向谷氨酰胺转运蛋白
- 抑制SLC1A5等转运蛋白会切断谷氨酰胺的供应,进一步限制生长。
-
免疫代谢和T细胞活化
- 谷氨酰胺在活化过程中帮助T细胞,并影响它们的功能。在免疫治疗的同时使用谷氨酰胺靶向治疗可以增强抗癌效果。
-
谷氨酰胺代谢的生物标记
- 跟踪谷氨酰胺相关标记物有助于个性化治疗。
-
组合方法
- 谷氨酰胺酶抑制剂与标准疗法相结合可能会提高疗效。这种策略还可以增加癌细胞对某些药物的敏感性。
-
平衡治疗和毒性
- GLS抑制剂可以选择性地靶向癌细胞,将对正常细胞的伤害降至最低。
-
饮食和谷氨酰胺摄入
- 减少饮食中的谷氨酰胺可能会增强治疗效果。然而,饮食、新陈代谢和治疗之间的关系是复杂的。
-
转移预防
- 靶向谷氨酰胺代谢可以通过限制细胞的适应能力来降低癌症扩散的风险。
9. 谷氨酰胺酶抑制剂的临床进展
谷氨酰胺酶抑制剂选择性地靶向癌细胞中过度活跃的GLS,放过正常细胞中的GLS2:
- 阻断上皮-间质转化:这些抑制剂有助于防止支持癌症扩散的EMT。
- 结合免疫疗法:因为谷氨酰胺为T细胞提供燃料,将抑制剂与免疫治疗配对可以增强抗癌效果。
10. 未来方向
- 新药筛选:自动化技术可以帮助找到更好的谷氨酰胺酶抑制剂。
- 精确医学:基于肿瘤代谢概况的定制治疗可以改善结果。
- 超越新陈代谢的探索:谷氨酰胺可能影响基因调节,提供新的治疗可能性。
11. 结论
谷氨酰胺代谢在癌细胞和免疫细胞如T细胞中起着至关重要的作用。它影响自噬和活性氧调节等过程,影响癌症的生长和存活。针对这一途径为癌症治疗提供了一个有希望的策略,特别是与其他治疗方法结合使用。随着研究的进展,更有效的方法将会出现。



